EGFRリキッドは、肺癌患者の血漿あるいは癌組織(未固定)から抽出したDNAを用いてEGFR変異(エクソン19欠失、L858R、参考としてT790M)の陽性陰性を判定し、EGFR-TKI治療方針決定の補助する遺伝子変異検査(医療機器プログラム)である。EGFRリキッドでは血漿DNAのEGFR遺伝子をPCR増幅し、次世代シーケンサーを用いて10万回以上配列決定を行って変異検索を行うため、微量な変異でも検出できる。臨床性能、すなわち臨床検体を用いた検査性能は、肺癌患者血漿検体と肺癌組織を用いた2つの相関性試験により確認している。
関連記事
「EGFR exon 19 deletion : エクソン19欠失 〜 サブタイプとキナーゼ活性化メカニズム」
「肺癌遺伝子検査に関する基本的な見解」
血漿検体と生検検体を比較する相関性試験
試験概要
EGFRリキッドのEGFR変異検査法としての妥当性を検証するため、生検組織検体をPNA-LNA PCR クランプ法で検出した結果との相関性を検証した。この試験は検体収集と変異検出を多施設前向き試験(UMIN-CTR 番号:UMIN000006762)として行った。本試験は単純な測定法の比較試験ではなく、実地臨床で生検代替が可能かどうか調べたものである。そのため生検と血液採取を同時に実施、生検の病理診で癌細胞を確認できた症例のみ集めている。
参加施設:大阪府立成人病センター、大阪市立総合医療センター、大阪大学医学部附属病院。
患者選択基準基準:前治療のない患者、ステージは問わない。
目標症例数:320症例。全体感度の95%信頼区間が20%以内になる症例数として設定。
検体収集基準:生検検体と血液検体を2週間以内の間隔で採取し、生検検体で癌細胞を確認したもののみ登録。
患者登録期間:2011年11月−2014年4月。
EGFRリキッドによる血漿EGFR変異率測定期間:2012年9月−2014年7月。
試験結果
目標320症例で321症例登録、検体欠落のため最終的に測定できた症例は288となった。相関性試験の結果を図1に示す。図1に基づき感度・特異度・全体感度(変異タイプを問わない感度)を算出した(図2)(注1)。T790Mは生検陽性症例がないため特異度のみ算出できる。エクソン19欠失あるいはL858R陽性症例103例中、検出限界が閾値の場合6例、定量限界の場合1例T790M陽性例があった。従って特異度は検出限界が閾値の場合94.2%(95%信頼区間87.6-97.6)、定量限界の場合99.0% (94.2 – 100)であった。定量限界と検出限界に関しては別の機会に説明する。
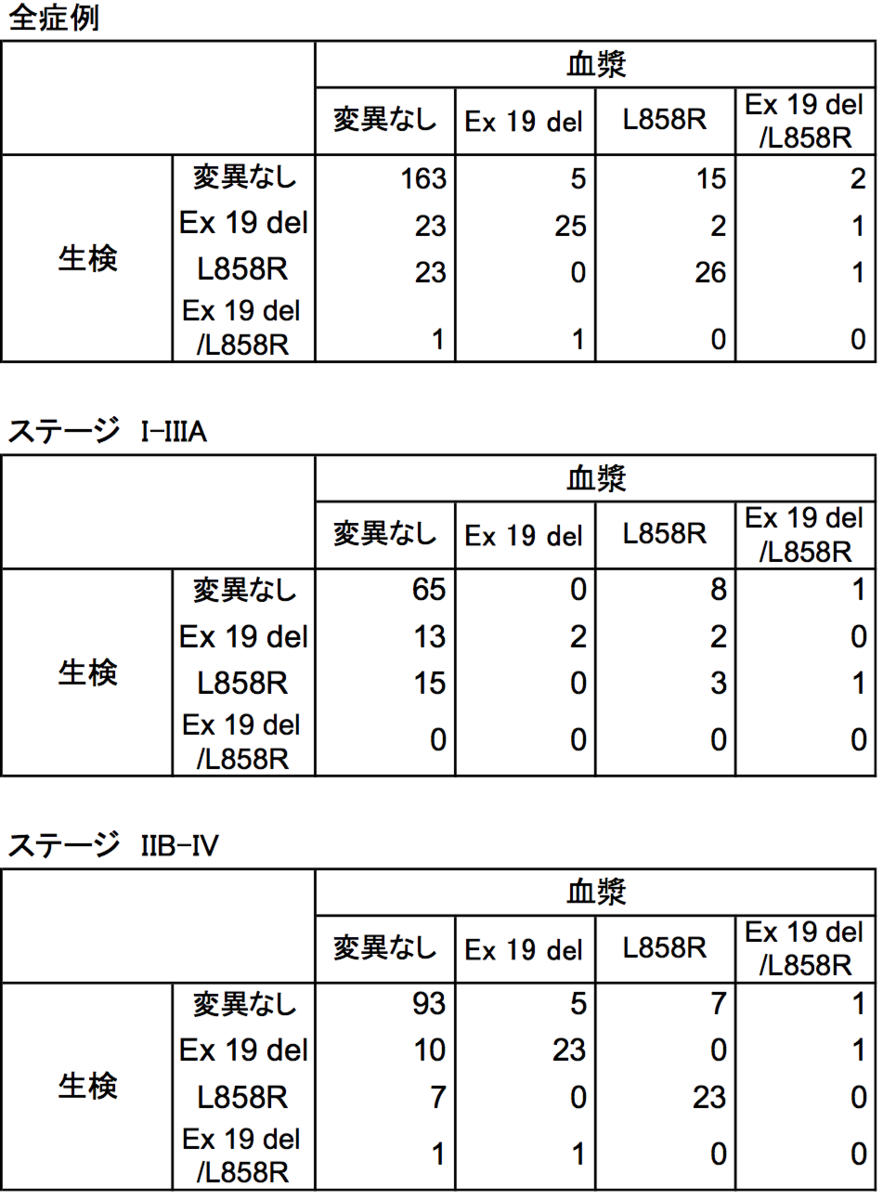
図1.血漿相関試験結果。
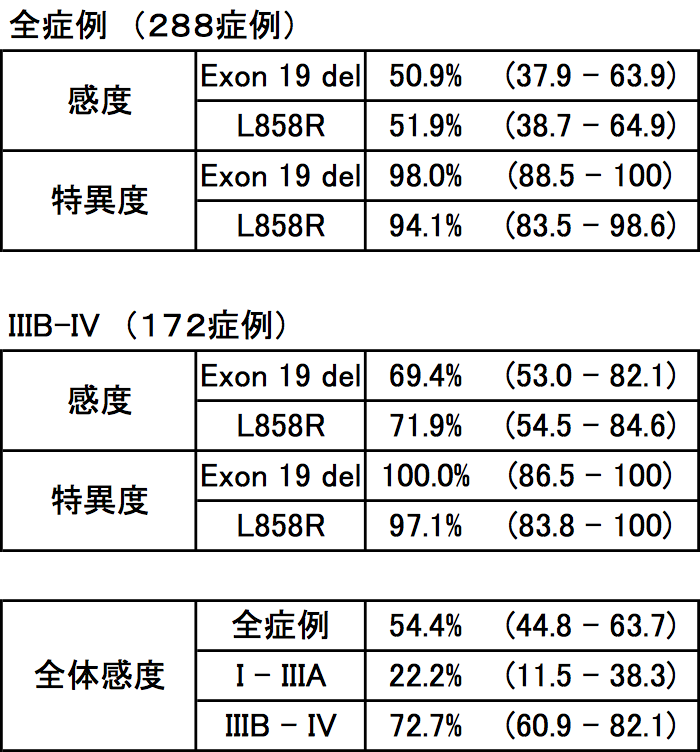
図2.血漿検体の生検検体に対する感度、特異度、全体感度。全体感度は変異タイプを問わない感度。
すべての変異で特異度が高いため、血漿での陽性結果で直接EGFR-TKI治療選択が可能である。全体感度はステージI-IIIAでは低いが、EGFR-TKI治療対象であるステージIIIB-IV(EGFR-TKI治療対象患者)では高い。後者に限定した解析を行った(表4. 3. 9. 3-3)。患者全体での解析より感度特異度とも点推定値が改善している。信頼区間についても損失はない。
相関性試験(肺癌組織・未固定)
試験概要
この試験では同一検体を用いてEGFRの変異検出法の性能を既存法(PNA-LNA PCRクランプ法)と比較した。検出技術そのものの評価である。
研究責任者:加藤菊也
試験実施場所:奈良先端科学技術大学院大学疾患ゲノム医学研究室
検討対象:手術摘出肺癌組織、凍結未固定。大阪府立成人病センター(現・大阪国際がんセンター)で1999〜2002年に手術摘出されたもの。156検体。
検出法:EGFRリキッドとPNA-LNA PCR クランプ法(LSI メディエンスで実施)。
試験期間:2018年7月5日 ~ 2018年9月29日。
試験結果
試験結果を図3に示す。EGFR変異陽性検体数は、クランプ法で51(32.9%)、EGFRリキッドで45(28.9%)と日本人集団としては若干出現率が低いが、許容範囲内である。変異全体の合致率が若干目標値より低いが、ほぼ設定した評価基準を満たしている。
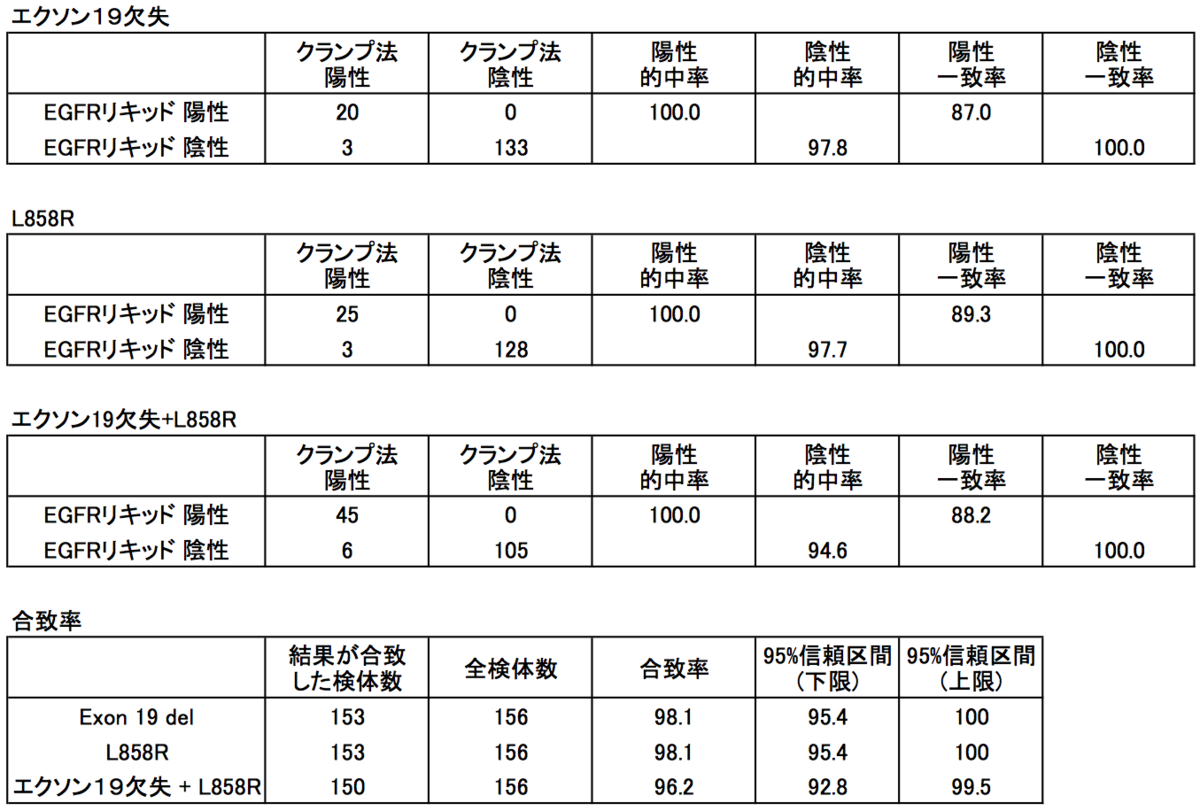
図3.肺癌組織検体(凍結未固定)相関試験結果。
不一致例はすべてクランプ法陽性EGFRリキッド陰性(エクソン19欠失3例、L858R 3例)であった。これら不一致例をコバスⓇEGFR変異検出キットv2.0を用いて測定した。L858RについてはPCR増幅バイアスによって変異アレルが消失した可能性を考慮し、鋳型DNA量を50 ng, 500 ngと増加させて再度解析した。これらの試験結果を表図4に示す。以前サンガー法で解析した変異型も掲載した。EGFRリキッド陰性6検体のうち、1検体を除いてすべてコバスⓇEGFR変異検出キット陰性であった。クランプ法とEGFRリキッドで結果が合致した検体はすべてコバスⓇでも同じ結果になる、と仮定すると、EGFRリキッドとコバスⓇEGFR変異検出キットの合致率は99.4%(155/156)、95%信頼区間は下限97.3%、上限100%となる。
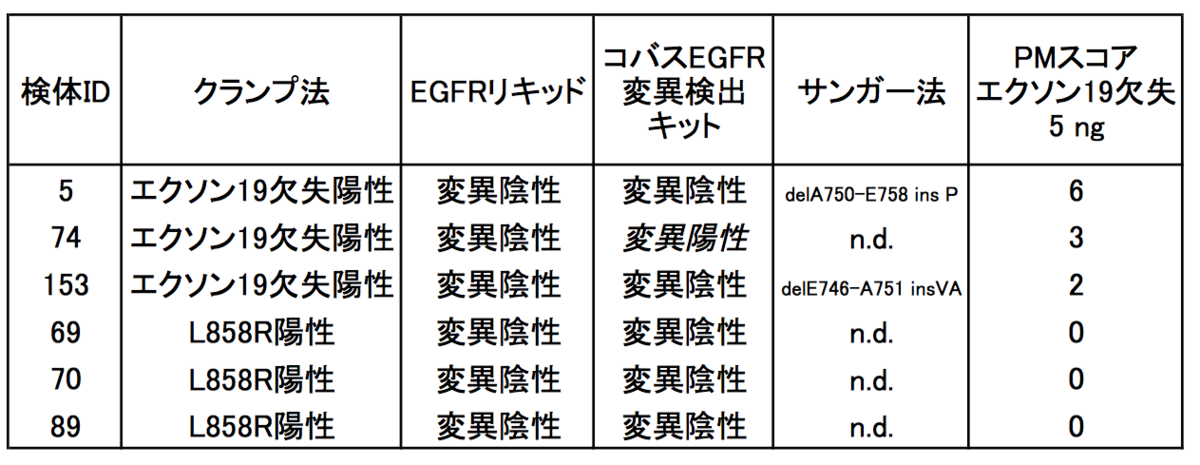
図4.不一致例の詳細解析。n.d., データなし。製品版ではdelE746-A751 insVAを追加している。
注1.感度・特異度の計算方法
全症例エクソン19欠失について計算法を説明する。
(感度)
血漿エクソン19欠失陽性例は
生検ex19 del 血漿 ex19 del 25例
生検ex19 del 血漿 ex19 del/L858R 1例
生検ex19 del/L858R 血漿 ex19 del 1例
の計27例になる。
生検エクソン19欠失陽性例は、これらに加えて
生検ex19 del 血漿 変異なし 23例
生検ex19 del 血漿 L858R 2例
生検ex19 del/L858R 血漿 変異なし 1例
であるため53例となる。したがって
感度 100x(25+2)/( 25+2+23+2+1)=50.9%。
(特異度)
生検検体陰性例は真に変異陰性の場合と測定に失敗して(腫瘍細胞採取の失敗が多い)陰性になる場合がある。感度の算出は生検検体陽性例を用いるため問題はおこらない。特異度算出に関しては測定の問題を回避するためにエクソン19欠失の特異度算出には生検L858R陽性例を、L858Rの特異度算出には生検エクソン19欠失陽性例を用いた。例で示したエクソン19欠失の場合分母の50例は
生検L858R陽性血漿変異なし 23例
生検L858R陽性血漿L858R 26例
生検L858R陽性血漿exon 19 del/L858R 1例
この50例中血漿でexon 19 del陽性例は血漿exon 19 del/L858Rの1例のみであるから分子は49になる。従って、
特異度 100x(1-(50-1)/50)=98.0%。
成果発表
(血漿検体)
Uchida, J., Kato, K., Kukita, Y., Kumagai, T., Nishino, K., Daga, H., Nagatomo, I., Inoue, T., Kimura, M., Oba, S., Ito, Y., Takeda, K. and Imamura, F. Diagnostic accuracy of noninvasive genotyping of EGFR in lung cancer patients using deep sequencing of plasma cell-free DNA. Clinical Chemistry, 51 (2015) 1191–1196. DOI: 10.1373/clinchem.2015.241414
(肺癌組織)
加藤菊也、岡見次郎、東山聖彦、今村文生. EGFRリキッド — EGFR変異解析プログラム. 第60回肺癌学会学術総会(2019年12月8日). https://www.haigan.gr.jp/journal/am/2019a/19a_gol500O50-4.html